Mit dem ARACUS Aminosäureanalysator wurde eine präzise Methode zur gleichzeitigen Bestimmung mehrerer diagnostisch relevanter Aminosäuren im Blutplasma entwickelt und validiert. Die Analyse umfasst Schlüsselmarker für Stoffwechselerkrankungen wie MSUD, Homocystinurie und PKU, darunter Homocystein, verzweigtkettige Aminosäuren und das Phenylalanin/Tyrosin-Verhältnis. Die Methode liefert eine zuverlässige Grundlage für das Screening, die Diagnose und die Verlaufskontrolle dieser genetischen Störungen.
Bestimmung der Aminosäuren als Biomarker für Stoffwechselerkrankungen mit dem ARACUS
Ziel der Studie war die Entwicklung und Validierung einer Methode zur Bestimmung der Aminosäuren Homocystein, Valin, Methionin, Allo-Isoleucin, Isoleucin, Leucin, Tyrosin und Phenylalanin im menschlichen Blutplasma in einem Durchgang. Die Ahornsirup-Urin-Krankheit (MSUD) ist eine der autosomal-rezessiv vererbten Stoffwechselerkrankungen, die die Aminosäuren Valin, Allo-Isoleucin, Isoleucin und Leucin betrifft. Ein erhöhter Homocysteinspiegel geht mit Homocystinurie einher, einer weiteren Stoffwechselerkrankung. Phenylketonurie (PKU) ist eine seltene Erbkrankheit, bei der der Körper die Aminosäure Phenylalanin nicht verstoffwechseln kann. Normalerweise wird sie verstoffwechselt und in die Aminosäure Tyrosin umgewandelt. Hohe Phenylalaninwerte sind schädlich für das Gehirn.
Probenvorbereitung und Analyse
500 µl Blutplasma und 100 µl 4%ige Dithiothreitol-Lösung wurden in einem 1,5-mL-Röhrchen gemischt und 30 Minuten lang bei 40° bebrütet. Gebundene Formen von Homocystein in der Probe werden durch die Verwendung von 4%iger Dithiothreitol-Lösung in Form von freiem Homocystein reduziert. Nach der Inkubation werden 150 µL der Fällungslösung zugegeben und für 20 min im Kühlschrank zur Proteinfällung gelagert. Dann wurden 500 µL Probenverdünnungspuffer (einschließlich des internen Standards Norleucin, 100 nmol/mL) zugegeben und gemischt. Der Überstand wurde mit einem membraSpin durch Zentrifugation bei 14000 rpm für fünf Minuten filtriert. Die partikelfreie Lösung wurde für die Injektion verwendet.
Die Proben wurden mit dem Amino Acid Analyzer ARACUS analysiert, der von der membraPure GmbH hergestellt und weltweit vertrieben wird. Der ARACUS verwendet die klassische Routineanalyse von Aminosäuren durch Nachsäulenderivatisierung mit Ninhydrin und die Detektion bei 440 nm und 570 nm.
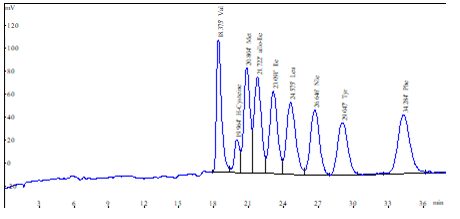
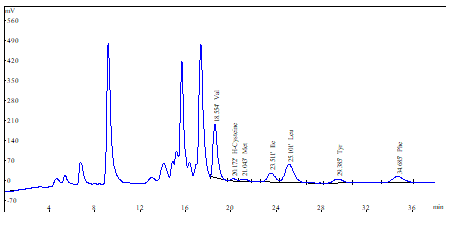
Ergebnisse und Diskussion
Tabelle 1 zeigt die Ergebnisse von Neugeborenen ohne MSUD. Tabelle 2 zeigt die Ergebnisse von Neugeborenen mit MSUD.
Tabelle 1: Aminosäurekonzentration von Valin (Val), Homocystein (H-Cystein), Methionin (Met), Allo-Isoleucin (Allo-Ile). Isoleucin (Ile). Leucin (Leu). Tyrosin (Tyr). und Phenylalanin (Phe) in nmol/mL Plasma von Neugeborenen ohne MSUD.
| Amino Acid | x̅ | SD |
| Val | 202.1 | ± 54.1 |
| H-Cystein | 4.4 | ± 1.5 |
| Met | 31.1 | ± 7.9 |
| allo-Ile | < 2 | – |
| Ile | 58.9 | ± 16.9 |
| Leu | 141.9 | ± 40.5 |
| Tyr | 108.1 | ± 31.2 |
| Phe | 99.4 | ± 18.6 |
Tabelle 2: Aminosäurekonzentration von Valin (Val). Homocystein (H-Cystein). Methionin (Met). Allo-Isoleucin (Allo-Ile). Isoleucin (Ile). Leucin (Leu). Tyrosin (Tyr) und Phenylalanin (Phe) in nmol/mL Plasma von Neugeborenen mit MSUD.
| Amino Acid | Mean x̅ | SD |
| Val | 467.9 | ± 116.9 |
| H-Cysteine | 6.9 | ± 2.8 |
| Met | 17.2 | ± 4.0 |
| allo-Ile | 66.2 | ± 27.4 |
| Ile | 213 | ± 48.6 |
| Leu | 433.6 | ± 108.1 |
| Tyr | 67.4 | ± 20.9 |
| Phe | 70.2 | ± 11.2 |
Die Ergebnisse zeigen, dass die Konzentrationen der Aminosäuren Valin, Allo-Isoleucin, Isoleucin und Leucin bei Neugeborenen mit MSUD ansteigen. Der normale Referenzbereich für Homocystein liegt bei 4,2 – 12,8 nmol/ml Plasma. Eine erhöhte Homocysteinkonzentration ist mit Homocystinurie assoziiert.
Ein positiver Neugeborenen-Screeningtest auf PKU muss durch eine quantitative Plasma-Aminosäurenanalyse weiterverfolgt werden, bei der die Konzentration von Phenylalanin und Tyrosin gemessen wird. Ein Phenylalaninwert im Blutplasma von mehr als 360 µM ist mit der Diagnose einer PKU vereinbar. PKU kann abnorm niedrige Werte von Tyrosin, einer nicht-essentiellen Aminosäure, verursachen.
Referenzwerte für Phenylalanin:
- Frühgeborene: 90-213 nmoL/mL
- 0-31 Tage: 38-137 nmoL/mL
- 1-24 Monate: 31-75 nmoL/mL
- 2-18 Jahre: 26-91 nmoL/mL
Referenzwerte für Tyrosin:
- Frühgeborene: 147-420 nmoL/mL
- 0-31 Tage: 55-147 nmoL/mL
- 1-24 Monate: 22-108 nmoL/mL
- 2-18 Jahre: 24-115 nmoL/mL
Für diese Studie stand derzeit kein Blutplasma eines Neugeborenen mit PKU zur Verfügung, aber der Anwendungshinweis zeigt, dass es mit der Methode möglich ist, alle Schlüsselkomponenten, die mit MSUD und PKU in Verbindung stehen, in einem einzigen Durchgang zu analysieren.
Validierung/Präzision
Die Präzision der Methode wurde durch die Wiederholbarkeit (innerhalb eines Tages) (Tabelle 3) und die mittlere Präzision (zwischen den Tagen) (Tabelle 4) bestimmt. Die Intra-Tages-Präzision wurde als relative Standardabweichung (RSD) der Ergebnisse von zehn Durchläufen der Probe am selben Tag berechnet. Die Zwischen-Tages-Präzision wurde durch eine tägliche Probenvorbereitung für zehn Mal über einen Zeitraum von zwei Wochen untersucht. Die Standardabweichung (SD) und die RSD wurden berechnet.
Tabelle 3: Intraday-Präzision von Aminosäuren im Blutplasma. Konzentration in mg/g (Injektion n=10).
| Amino Acid | Mean x̅ | SD | RSD / % |
| H-Cys | 7.34 | ± 0.305 | 4.15 |
| Val | 164.4 | ± 0.855 | 0.52 |
| Met | 20.87 | ± 0.244 | 1.17 |
| Ile | 46.22 | ± 0.269 | 0.58 |
| Leu | 107.2 | ± 0.586 | 0.55 |
| Nle | 99.53 | ± 0.607 | 0.61 |
| Tyr | 67.8 | ± 0.380 | 0.56 |
| Phe | 69.1 | ± 0.511 | 0.73 |
Tabelle 4: Inter-Tages-Präzision der Aminosäuren im Blutplasma. Konzentration in mg/g (Injektion n=10).
| Amino Acid | Mean x̅ | SD | RSD / % |
| H-Cys | 7.56 | ± 0.436 | 5.77 |
| Val | 163.8 | ± 2.172 | 1.33 |
| Met | 21.24 | ± 0.592 | 2.76 |
| Ile | 44.67 | ± 0.908 | 2.03 |
| Leu | 105.3 | ± 1.721 | 1.63 |
| Nle | 100.37 | ± 1.141 | 1.13 |
| Tyr | 69.13 | ± 0.830 | 1.2 |
| Phe | 70.35 | ± 0.617 | 0.88 |
Genauigkeit (Wiederherstellung)
In dieser Validierungsstudie wurde die Genauigkeit der Methode durch Berechnung der Wiederherstellungswerte (Tabelle 6) untersucht, die durch Analyse der mit Homocystein-Standard (40 nmol/mL) aufgestockten Plasmaprobe erhalten wurden. Zur Herstellung der Stammlösung für die serielle Verdünnung wurden 2 mL Homocysteinstandard zu 2 mL Blutplasma gegeben. Das Schema der seriellen Verdünnungsproben, die 100%, 80%, 60%, 40%, 20% und 10% entsprechen, ist in Tabelle 5 dargestellt.
Tabelle 5: Schema der seriellen Verdünnungsproben
| Plasma sample concentration/ % | Plasma sample / µL | Sample dilution buffer / µL |
| 100 | 1000 | – |
| 80 | 800 | 200 |
| 60 | 600 | 400 |
| 40 | 400 | 600 |
| 20 | 200 | 800 |
| 10 | 100 | 900 |
Linearität
Die Linearität ist wichtig für die Bestätigung der Empfindlichkeit der Methode bei der Analyse der Aminosäurekonzentration innerhalb eines bestimmten Bereichs.
Die Linearität ist die Fähigkeit, Testergebnisse zu erhalten, die direkt proportional zur Konzentration der Aminosäure sind. Die Linearität wurde durch fünf Injektionen von sechs verschiedenen Konzentrationen (5, 10, 20, 30, 40 und 50 nmol/mL) bestimmt. Die durchschnittlichen Peakflächen wurden gegen die Konzentrationen aufgetragen. Anschließend wurde die Linearität anhand der Kalibrierungskurve bewertet, um Korrelationskoeffizient, Steigung und Achsenabschnitt zu berechnen (Tabelle 7). Im Allgemeinen wird ein Korrelationskoeffizient (R2) > 0,990 als Beweis für eine akzeptable Anpassung der Daten an die Regressionslinie angesehen.
Tabelle 6: Wiederherstellungswerte für Verdünnungsreihen für jede Aminosäure, die in nmol/ml Blutplasma analysiert wurden (Injektion n=10).
| blood plasma | ||||||
| Run | 100% | 80% | 60% | 40% | 20% | 10% |
| H-Cys | ||||||
| mean x̅ | 43.48 | 35.21 | 26.0 | 17.15 | 8.77 | 4.26 |
| SD | ± 0.308 | ± 0.267 | ± 0.175 | ± 0.494 | ± 0.0898 | ± 0.0975 |
| RSD % | 0.71 | 0.76 | 0.67 | 2.88 | 1.02 | 2.29 |
| Recovery % | – | 80.98 | 59.8 | 39.43 | 20.23 | 9.79 |
| Val | ||||||
| mean x̅ | 166.8 | 132.8 | 103.7 | 67.43 | 32.39 | 16.72 |
| SD | ± 0.739 | ± 0.83 | ± 0.452 | ± 0.256 | ± 0.12 | ± 0.148 |
| RSD % | 0.44 | 0.63 | 0.44 | 0.38 | 0.37 | 0.89 |
| Recovery % | – | 79.62 | 62.16 | 40.43 | 20.62 | 10.02 |
| Met | ||||||
| mean x̅ | 21.99 | 17.4 | 13.62 | 8.95 | 4.54 | 2.21 |
| SD | ± 0.154 | ± 0.201 | ± 0.149 | ± 0.0368 | ± 0.051 | ± 0.0272 |
| RSD % | 0.154 | 1.16 | 1.09 | 0.41 | 1.12 | 1.23 |
| Recovery % | – | 79.12 | 61.94 | 40.7 | 20.65 | 10.05 |
| Ile | ||||||
| mean x̅ | 44.75 | 35.55 | 27.84 | 18.4 | 9.5 | 4.79 |
| SD | ± 0.213 | ± 0.228 | ± 0.276 | ± 0.088 | ± 0.085 | ± 0.084 |
| RSD % | 0.48 | 0.64 | 0.99 | 0.48 | 0.89 | 1.75 |
| Recovery % | – | 79.44 | 62.21 | 41.12 | 21.23 | 10.71 |
| Leu | ||||||
| mean x̅ | 109.3 | 87.36 | 68.06 | 44.27 | 22.56 | 11.05 |
| SD | ± 0.591 | ± 0.459 | ± 0.642 | ± 0.196 | ± 0.199 | ± 0.109 |
| RSD % | 0.54 | 0.53 | 0.94 | 0.44 | 0.88 | 0.98 |
| Recovery % | – | 79.54 | 61.97 | 40.31 | 20.54 | 10.6 |
| Tyr | ||||||
| mean x̅ | 69.89 | 54.71 | 43.44 | 28.87 | 14.81 | 7.17 |
| SD | ± 0.412 | ± 0.346 | ± 0.442 | ± 0.154 | ± 0.223 | ± 0.145 |
| RSD % | 0.59 | 0.63 | 1.02 | 0.53 | 1.51 | 2.02 |
| Recovery % | – | 78.28 | 62.15 | 41.31 | 21.19 | 10.26 |
| Phe | ||||||
| mean x̅ | 69.12 | 55.12 | 43.09 | 28.79 | 14.79 | 7.76 |
| SD | ± 0.474 | ± 0.382 | ± 0.438 | ± 0.152 | ± 0.151 | ± 0.125 |
| RSD % | 0.69 | 0.69 | 1.02 | 0.53 | 1.02 | 1.61 |
| Recovery % | – | 79.74 | 62.34 | 41.65 | 21.4 | 11.23 |
Tabelle 7: Linearität der durchschnittlichen Peakfläche gegen verschiedene Aminosäurekonzentrationen.
| Amino Acid | R² |
| H-Cys | 0.9983 |
| Val | 0.9997 |
| Met | 0.9998 |
| Ile | 0.9999 |
| Leu | 0.9999 |
| Nle | 0.9998 |
| Tyr | 0.9999 |
| Phe | 0.9998 |
Table 8: Limit of detection and limit of qualification for each amino acid, analysed in blood plasma.
| Amino Acid | LOD nmoL/mL | LOQ nmol/mL |
| H-Cys | 0.82 | 2.46 |
| Val | 0.74 | 2.22 |
| Met | 0.84 | 2.52 |
| Ile | 0.83 | 2.49 |
| Leu | 0.76 | 2.28 |
| Nle | 0.8 | 2.4 |
| Tyr | 0.76 | 2.28 |
| Phe | 0.89 | 2.27 |
LOD & LOQ
Die Nachweisgrenze (LOD) ist die kleinste Menge oder Konzentration der Aminosäure in der Probe, die zuverlässig von Null unterschieden werden kann.
Bestimmen Sie den Mittelwert und die Standardabweichung (SD) von zehn unabhängigen Messungen einer Blindprobe oder einer Probe mit sehr geringen Konzentrationen der Messgröße.
Nachweisgrenze LOD = x̅ + 3 SD.
Die Bestimmungsgrenze (LOQ) ist die niedrigste Konzentration der Aminosäure, die unter den festgelegten Akzeptanzkriterien mit Genauigkeit und Präzision quantitativ bestimmt werden kann.
Bestimmungsgrenze LOQ = 3 LOD.
Hinweis: Die zu diesem Artikel gehörige PDF ist zum Download nur auf Englisch verfügbar.
Quellen:
- Refsum H. et. al. Screening for Serum Total Homocysteine in Newborn Children. Clinical Chemistry 50. No. 10. 2004 .
- Schadewaldt P. et al Significance of L-allo-isoleucine in plasma for diagnosis of maple syrup urine disease. Clin Chem. 1999 Oct; 45(10):1734-40.
- D. Timmermann, E. Flindt, EP3596474B1, Method for the chromatographic quantitative determination of the amino acids Valine, Methionine, allo-Isoleucine, Isoleucine, Leucine, Tyrosine and Phenylalanine in blood plasma.

